Conduta na Isoimunização Rh
A Isoimunização Rh, Doença Hemolítica Perinatal (DHPN) ou eritroblastose fetal é uma afecção generalizada que consiste na hemólise do sangue fetal. É decorrente da produção materna de anticorpos IgG contra hemácias do feto.
A incidência é de 1 a 6 gestações por 1000 recém nascidos vivos. Cerca de 98% dos casos de isoimunização materna na DHPN são devidos ao fator Rh(D). Os restantes 2%, a antígenos atípicos como os fatores Kell, E ou c.
As membranas dos glóbulos vermelhos contêm numerosos antígenos de superfície incluindo os dos grupos ABO e Rhesus. A exposição inicial ao antígeno das hemácias desencadeia uma resposta imune primária fraca na mãe, resultando na produção de IgM após um período latente de algumas semanas. Visto que a IgM não pode atravessar a placenta, o feto não é acometido.
Em exposição subseqüente da mãe a glóbulos vermelhos antigênicos semelhantes (freqüentemente em uma gravidez subseqüente) suas células B de memória previamente produzidas agem rapidamente para produzir anticorpos IgG. Os anticorpos IgG maternos são transportados ativamente através da placenta atingindo os glóbulos vermelhos fetais que expressarem aquele antígeno, causando então seu seqüestro e posterior fagocitose e/ou citólise.
Conduta no pré-natal
Todas as gestantes deverão realizar rotineiramente tipagem sanguínea ABO e fator Rh. As pacientes com fator Rh negativo deverão obrigatoriamente realizar teste de Coombs indireto o mais breve possível.
Nas pacientes Rh negativo, com teste de Coombs indireto também negativo deverá ser repetido o teste de Coombs indireto a cada trimestre. Na 28a. semana de gestação estas pacientes deverão receber uma dose de imunoglobulina anti-D. Após a realização da imunoglobulina anti-D espera-se que o teste de Coombs indireto fique positivo, porém com títulos baixos (até 1:16) e que devem negativar em cerca de 3 meses. Portanto, após a realização da imunoglobulina não é mais necessário o teste de Coombs indireto. Após o parto deve ser realizada a tipagem sanguínea do recém-nascido e na eventualidade deste ser Rh positivo uma nova dose de imunoglobulina anti-D deverá ser administrada na mãe em até 72 horas após o parto.
As pacientes Rh negativo com teste de Coombs indireto positivo são consideradas isoimunizadas e o feto tem risco potencial de desenvolver a DHPN. Portanto estas gestações necessitam de avaliação com relação ao risco de anemia fetal.
Historicamente a avaliação do comprometimento fetal era realizada por meio da dosagem de bilirrubinas no líquido amniótico. Atualmente o grau de comprometimento fetal pode ser estimado pela velocidade do fluxo sanguíneo na artéria cerebral média com acurácia semelhante. Esta avaliação baseia-se no fato de que em virtude da anemia fetal ocorre a redução da viscosidade sanguínea e consequente aumento da velocidade de fluxo.
Para determinar a velocidade de pico sistólico da artéria cerebral média, inicialmente deve-se obter uma secção transversal do cérebro fetal, incluindo o tálamo e o cavo do septo pelúcido. Ligando-se o Doppler Color o polígono de Willis é visualizado e uma amostra da artéria cerebral media é analizada pelo Doppler Pulsado, próxima a sua origem na artéria carótida. O ângulo entre o feixe de ultrassom e a direção do sangue deve ser mantida o mais próximo possível de 0o. Caso a angulação seja maior que 0o, fazer a correção de ângulo. Na eventualidade da amostra obtida apresentar angulação maior que 30o, despreza-se a amostra e inicia-se novamente tentando reduzir o ângulo. Após a obtenção de uma amostra adequada mede-se o ponto mais alto da onda de variação de fluxo (pico de velocidade sistólica).
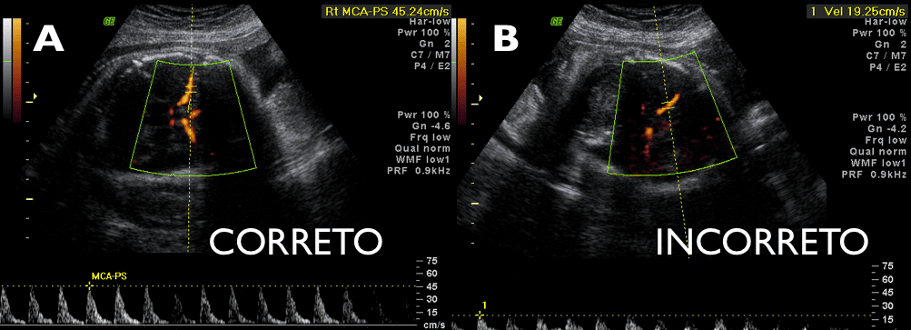
Modos correto e incorreto de medir o pico de velocidade sistólica da artéria cerebral média. O ângulo deve estar próximo de zero, com em A.
A velocidade encontrada no exame deverá ser dividida pela mediana da velocidade esperada para a idade gestacional, conforme os valores esperados para o Pico de Velocidade Sistólica da ACM. Velocidades acima de 1,5 múltipos da mediana (MdM) são sugestivas de anemia fetal grave (hemoglobina fetal abaixo de 8 mg/dl). Para determinar se o feto está anêmico ou não você pode usar nossa calculadora de pico sistólico da ACM.
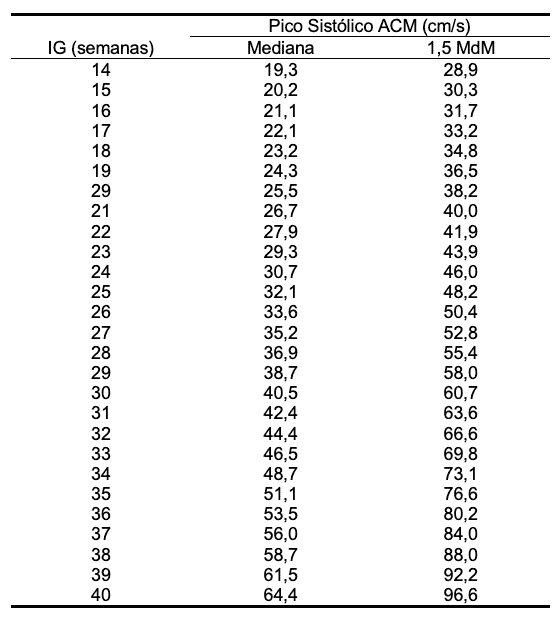
Tabela com o pico de velocidade sistólica da artéria cerebral média.
A conduta a ser seguida deve orientada pelo algoritmo abaixo:
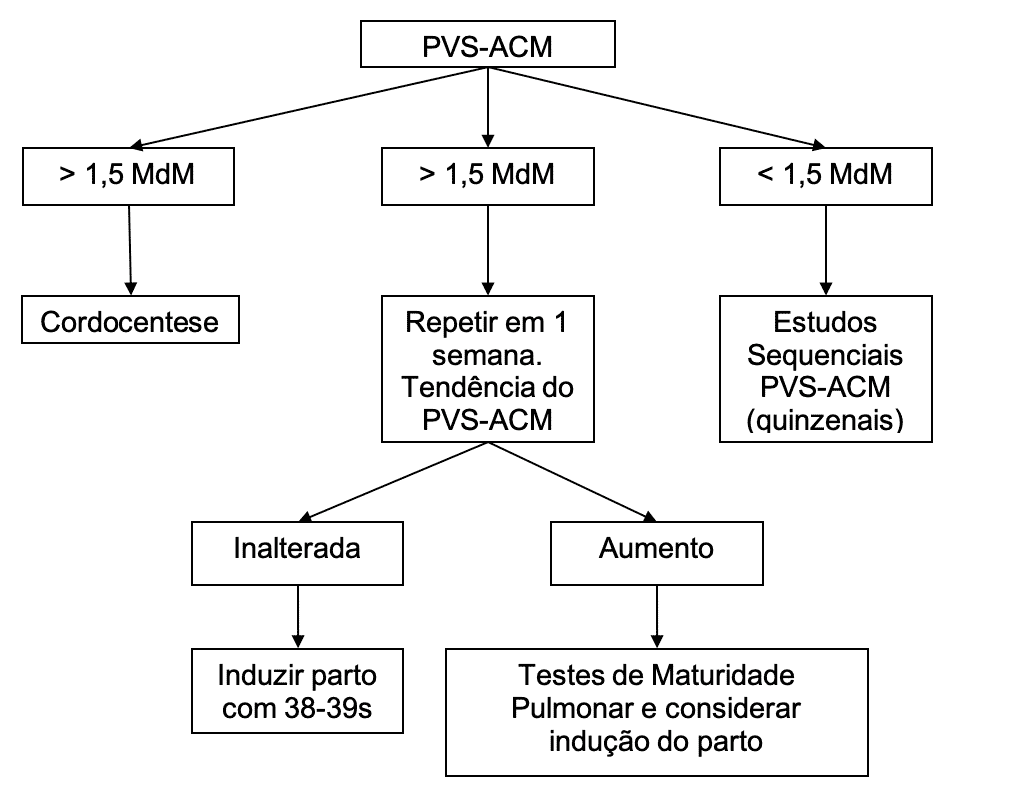
Conduta em pacientes isoimunizadas, segundo a velocidade de pico sistólico da artéria cerebral média. Adaptado de Mari et al.
Alguns achados ultrassonográficos são típicos de doença hemolítica com grave comprometimento fetal, entre eles podemos citar: ascite, derrames, polidrâmnio e placentomegalia. Estes achados estão presentes quando a hemoglobina fetal encontra-se abaixo de 4 mg/dl, sendo portanto achados mais tardios que a alteração de velocidade na artéria cerebral média.
Cordocentese em Fetos com Risco de Anemia Grave
Nas situações aonde houverem indícios de anemia fetal grave deverá ser realizada cordocentese. O procedimento poderá ser realizado ambulatorialmente ou com paciente internada. Sempre deverá ser feita reserva de 150 a 200 ml de sangue O negativo filtrado, lavado e irradiado e cruzado com o sangue materno. A equipe da neonatologia deverá ser informada antes do início das transfusões.
Após a realização da cordocentese uma amosta de 7 a 10 ml de sangue fetal será coletada para os seguintes exames:
- Tipagem sanguínea com fator Rh
- Hematócrito pré-transfusional (a ser realizado rapidamente no banco de sangue)
- Hemograma completo
- Contagem de plaquetas
- Coombs direto
- Bilirrubina total e frações
Havendo necessidade de transfusão a mesma deverá ser realizada no mesmo procedimento, com o objetivo de elevar o hematócrito pós-transfusional para 45.
As transfusões subsequentes deverão ser realizadas a cada 1 a 3 semanas, até a 34 semana de gestação momento em que deverá se considerar a resolução da mesma, preferencialmente com hemoglobina fetal acima de 10 mg/dl.
Em função das diferentes características físico-quimicas do sangue transfundido, o pico sistólico da artéria cerebral média apresenta maior número de falsos positivos, conforme o número de transfusões. Desta forma, recomendamos que o ponto de corte para a segunda transfusão seja 1,69 e as transfusões subsequentes deverão ser programadas conforme a queda da hemoglobina. Espera-se que a hemoglobina fetal caia cerca de 0,3 mg/dl/dia após as transfusões.
Cerca de 10 dias antes do parto, a paciente deverá iniciar o uso de fenobarbital 30 mg/dia, utilizado de maneira contínua até o parto.
Profilaxia da Isoimunização
Uma hemorragia feto-materna suficiente para causar isoimunização ocorre mais comumente durante o parto. A maioria das hemorragias são de menos de 0,1 ml a 0,2ml; 1% são maiores de 30 ml. A quantidade de hemorragia feto-materna necessária para causar isoimunização varia de acordo com a capacidade imunogênica das hemácias e com a resposta imune da mãe.
A imunoglobulina Rh(D) deve ser administrada via intramuscular a fim de prevenir a imunização ativa. São administrados 300μg dentro de 72 horas após o nascimento ou hemorragia feto-materna. O tempo limite de 72 horas é um artefato de metodologia de estudo. A administração da imunoglobulina até 14 a 28 dias pós-parto pode ser efetiva na prevenção da isoimunização.
No total, 16% das mulheres Rh-negativas tornam-se isoimunizadas em sua primeira gestação Rh-incompatível se não tratadas com imunoglobulina. Esse índice diminui a 1,5% se for administrada a imunoglobulina dentro de 72 horas após o nascimento, e diminui até 0,1% se a profilaxia for realizada também com 28 semanas de gestação. Outras indicações da imunoglobulina Rh(D) e a dose recomentada para cada uma são as seguintes:
- Abortamento no primeiro trimestre ou biópsia de vilo coriônico, administrar 50μg
- Gestação ectópica; administrar 300μg
- Amniocentese ou biópsia de vilo coriônico no segundo ou terceiro trimestre; administrar 300μg
- Hemorragia feto-materna (ex: sangramentos durante a gestação); administrar 10μg por cada ml de sangue fetal total estimado. A quantificação da hemorragia feto-materna requer uma amostra de sangue materno para o teste de Kleihaur-Betke. Este teste informa a porcentagem de hemácias fetais no sangue materno. Para determinar a quantidade de hemorragia feto-materna a porcentagem de hemácias fetais é multiplicada pelo volume sanguíneo materno e o produto é então multiplicado pelo hematócrito materno; o produto final representa o volume de hemácias fetais na circulação materna.
Assitência ao Parto de Rh Negativo Não Sensibilizada
Evitar manobras que aumentam os riscos ou a intensidade de hemorragia feto-materna: dequitação manual da placenta, tração ou torção de cordão umbilical previamente à dequitação, ordenha etc.
Referências
- Oepkes D, Seaward PG, Vandenbussche FPH a, Windrim R, Kingdom J, Beyene J, et al. Doppler ultrasonography versus amniocentesis to predict fetal anemia. The New England journal of medicine [Internet]. 2006 Jul;355(2):156–64.
- Mari G, Zimmermann R, Moise KJ, Deter RL. Correlation between middle cerebral artery peak systolic velocity and fetal hemoglobin after 2 previous intrauterine transfusions. American journal of obstetrics and gynecology [Internet]. 2005 Sep [cited 2013 Sep 14];193(3 Pt 2):1117–20.
- Scheier M, Hernandez-Andrade E, Fonseca EB, Nicolaides KH. Prediction of severe fetal anemia in red blood cell alloimmunization after previous intrauterine transfusions. American journal of obstetrics and gynecology [Internet]. 2006 Dec [cited 2013 Sep 14];195(6):1550–6.
- Detti L, Oz U, Guney I, Ferguson JE, Bahado-Singh RO, Mari G. Doppler ultrasound velocimetry for timing the second intrauterine transfusion in fetuses with anemia from red cell alloimmunization. American journal of obstetrics and gynecology [Internet]. 2001 Nov;185(5):1048–51.