O que é endometriose?
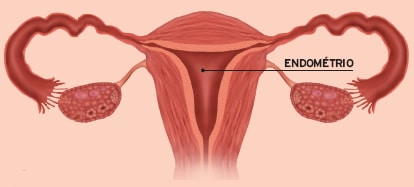
 O útero de toda mulher é revestido, internamente, por uma camada de tecido chamado endométrio, local onde o óvulo, quando fecundado, implanta-se para iniciar a gravidez (nidação). Caso a gravidez não ocorra, esta camada é expelida e exterioriza-se pela vagina através da menstruação. Em algumas mulheres, algumas células ou fragmentos deste endométrio são encontrados em outros órgãos, fora do útero, causando a endometriose.
O útero de toda mulher é revestido, internamente, por uma camada de tecido chamado endométrio, local onde o óvulo, quando fecundado, implanta-se para iniciar a gravidez (nidação). Caso a gravidez não ocorra, esta camada é expelida e exterioriza-se pela vagina através da menstruação. Em algumas mulheres, algumas células ou fragmentos deste endométrio são encontrados em outros órgãos, fora do útero, causando a endometriose.
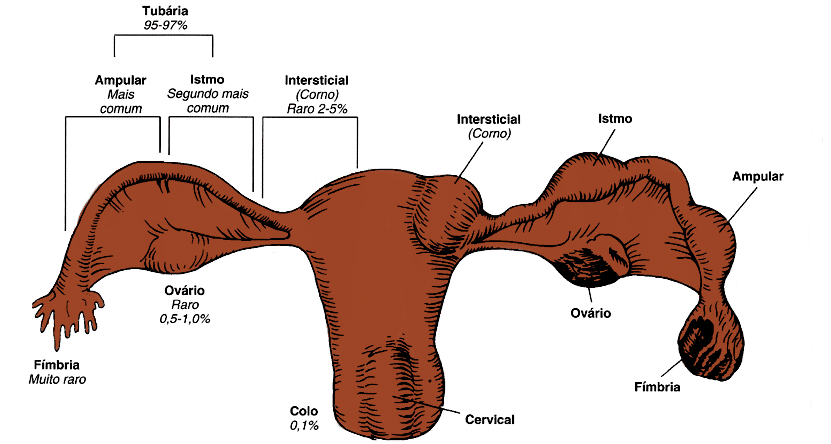
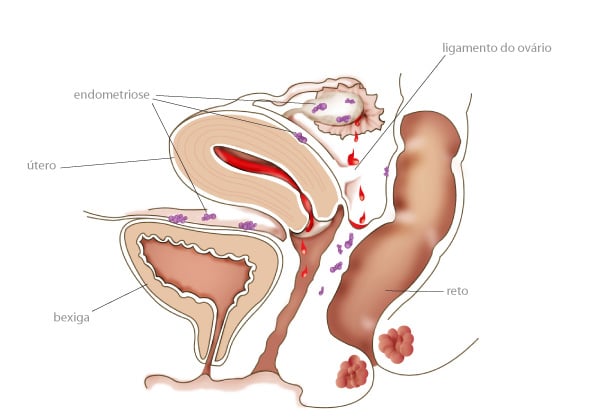
Estes focos de endométrio podem estar presentes mais comumente nos ovários, tubas uterinas, ligamentos que sustentam o útero. Também podem acometer a área entre a vagina e o reto (septo retovaginal), a superfície externa ou na musculatura do útero (adenomiose) e o revestimento da cavidade pélvica (peritôneo). Em alguns casos, também pode atingir outros órgãos. Por exemplo bexiga, intestino, vagina, colo do útero, vulva e cicatrizes cirúrgicas abdominais. As lesões mais profundas são chamadas de endometriose profunda (EP) ou infiltrativa. Para pesquisa de endometriose profunda o exame transvaginal habitualmente realizado não é suficiente, sendo mais indicado um exame chamado mapeamento ou pesquisa de endometriose.
Durante o ciclo menstrual, estes focos de endométrio fora do útero, também sofrem a ação dos hormônios (estrógeno e progesterona) e irão se comportar como se estivessem dentro do útero. Em outras palavras, estes focos crescem, se desenvolvem, ficam cheios de sangue e depois descamam. Porém, este sangue não tem para onde sair e fica acumulado dentro do abdome causando muita inflamação, dores e aderências.
Causas da Endometriose
As causas da endometriose ainda não são totalmente conhecidas. As mais prováveis são a genética e o fluxo menstrual retrógrado. Por exemplo o refluxo de uma pequena quantidade de sangue menstrual pelas trompas uterinas.
As principais características comportamentais da mulher moderna que predispõe à doença são, sem dúvida, a idade cada vez mais tardia da maternidade e o pequeno número de gestações, fatos cada vez mais frequentes. Nos dias de hoje, uma mulher está submetida na sua idade fértil a muito mais ciclos menstruais do que as mulheres do início do século passado. Antigamente tinha-se um maior número de gestações. Além disso a mulher de hoje é exposta a maior carga de trabalho e ansiedade. Por exemplo ao disputar o mercado de trabalho com o sexo masculino sem deixar de lado as responsabilidades da família. Isto gera maior nível de estresse e torna a endometriose o mal da mulher moderna.
Costuma provocar cólicas menstruais intensas (dismenorréia), dor pélvica importante, sangramento abundante ou irregular, ou outros sintomas durante as menstruações como náuseas, diarreia, sangue nas fezes, dificuldade de evacuar ou urinar e infertilidade são alguns dos sinais da endometriose. Mas os principais sintomas da doença são a dor durante a menstruação (dismenorréia) e no ato sexual (dispareunia). A endometriose costuma ser bastante sintomática e a profundidade da infiltração está relacionada com o tipo e a severidade dos sintomas. Para ter uma idéia de como a dor pode ser intensa, veja o post A dor da Endometriose Ilustrada.
Como diagnosticar a endometriose?
O diagnóstico pode ser suspeitado pela história clínica. O exame físico é importante principalmente na presença de lesões vaginais, retrocervicais e de ligamentos uterossacros. Porém para o diagnóstico de lesões localizadas em porções mais altas da pelve, nas alças intestinais e no fundo de saco de Douglas necessita de método de imagem complementar.
Apenas cerca de 10% das mulheres não têm sintomas. Isto pode fazer com que a doença evolua e aumente as chances de prejuízo à fertilidade da mulher. Gerando problemas para engravidar devido ao diagnóstico tardio.
Antes de descobrir que têm endometriose, é muito comum que as mulheres passem por um longo período de sofrimento. Infelizmente, o tempo médio entre o início dos sintomas e o diagnóstico da doença segundo estudos é de cerca de sete anos. Por isso é fundamental aumentar o conhecimento das mulheres a respeito da doença. Estudos indicam que 50% das mulheres que têm endometriose não conseguem engravidar. Só quando buscam ajuda médica para ter filhos, descobrem que são portadoras da doença.
A endometriose pode gerar infertilidade pelo acometimento das trompas. Elas que conduzem o óvulo ao útero. Além disso a endometriose poder se associar a alterações hormonais e imunológicas que dificultam a gestação.
A melhor prevenção é a mulher ficar atenta à dor, seja durante a menstruação ou nas relações sexuais. E procurar um médico ginecologista o mais rápido possível. Pois quanto mais cedo se detecta a doença, mais rápido um tratamento adequado poderá ser iniciado.
Como é feito o diagnóstico?
Exames complementares como a ultrassonografia pélvica transvaginal com preparo intestinal (mapeamento de endometriose) tem se mostrado exame preferencial para iniciar a investigação da endometriose profunda, visando a determinação da localização das lesões e do grau de profundidade do acometimento, avaliação decisiva para um planejamento terapêutico adequado.
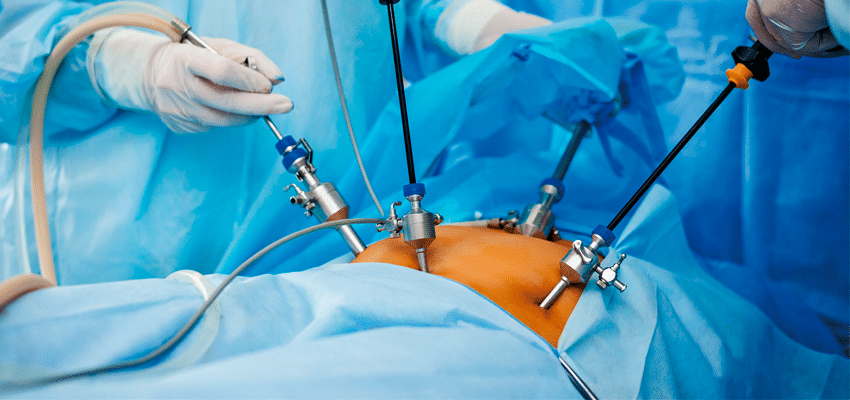
Hoje, a endometriose pode ser tratada de duas formas: cirurgicamente, por meio de laparoscopia, ou por meio de medicações, que bloqueiam a produção dos hormônios femininos, responsáveis pelo ciclo menstrual.