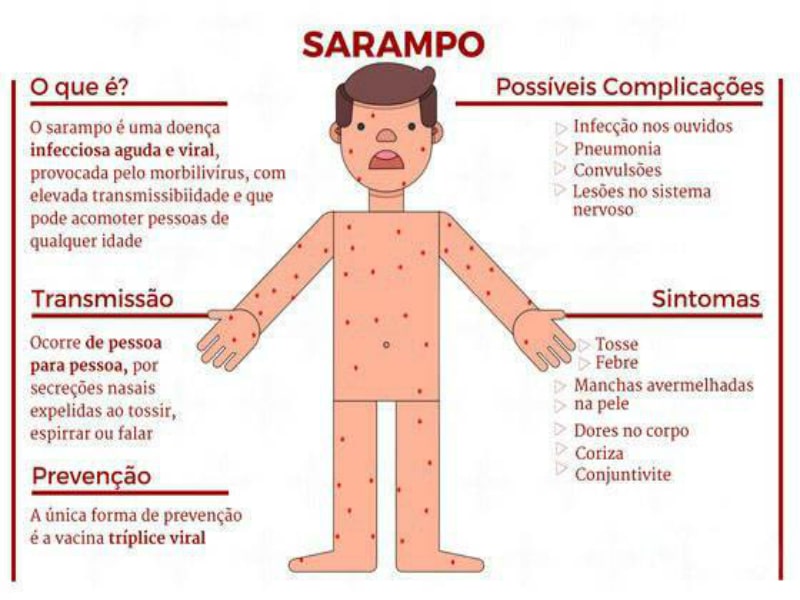
O sarampo é uma doença causada por um vírus, tem alto contágio e acomete principalmente crianças de até 5 anos de idade. Apesar de ser mais comum em crianças os adultos também podem contrair a doença. O sarampo na gravidez é particularmente grave pois poderá trazer riscos para a saúde da gestante e do bebê.
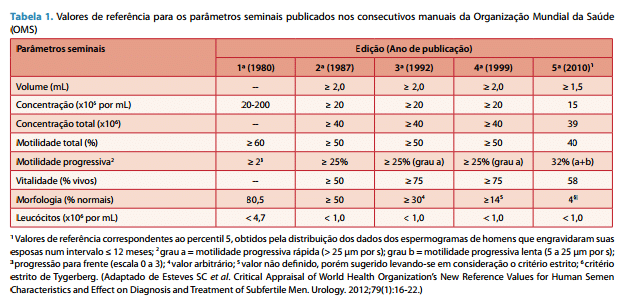
Embora exista uma vacina para a doença, em 2017 houve ainda 110 mil mortes por sarampo no mundo. A vacina, disponível desde 1963, foi aplicada em cerca de 85% das crianças no mundo no ano de 2017. Apesar desse número de crianças imunizadas ser alto, estima-se que 92 a 95% dos indivíduos de uma comunidade devem estar imunizados para evitar a transmissão da doença. Imunizar uma criança contra o sarampo custa menos de US$ 1,00!
Surto de Sarampo no Brasil
De 2015 a 2017 o Brasil não registrou nenhum caso da doença. Recentemente houve um fluxo intenso de imigrantes vindos da Venezuela para regiões da Amazônia e Roraima. De acordo com o Informe 36 do Ministério da Saúde, cerca de 10 mil casos já foram confirmados no Brasil.
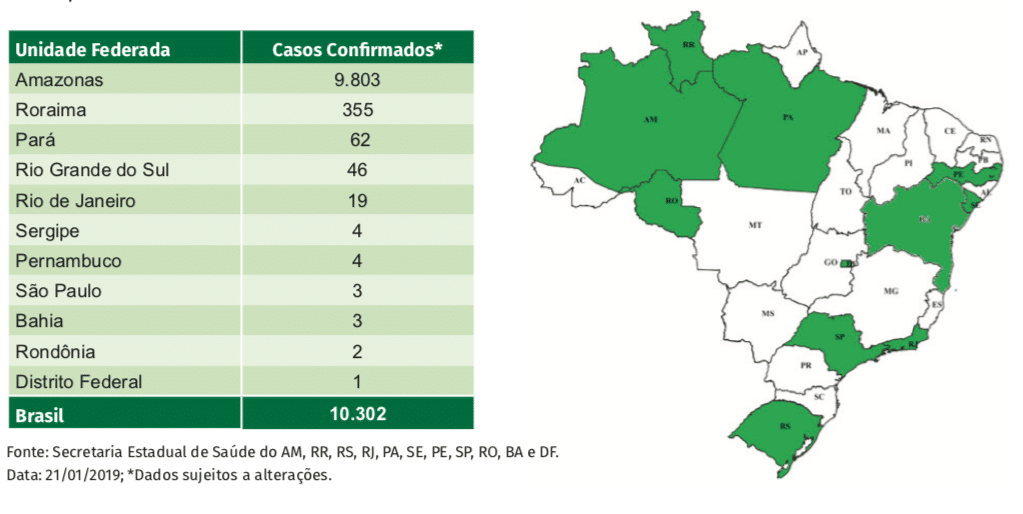
Em 2019, a cidade São Paulo virou um dos grandes focos de surto. Tem-se investido em uma grande campanha de vacinação e ampliado a indicação da imunização para pessoas de 15 a 29 anos, independentemente de elas já terem sido vacinadas. Bebês também podem ser vacinados a partir de 6 meses de idade. Segundo dados da OMS (Organização Mundial da Saúde), o avanço do sarampo é um fenômeno global, e nos últimos dois anos houve um aumento de 300% nos casos, comparados ao mesmo período em 2018.
O Brasil está na lista dos países mais afetados. A causa dessa mudança varia de acordo com cada nação, mas todas elas têm um ponto em comum: as pessoas estão deixando de se vacinar, apesar de a vacina ser a melhor forma de prevenir a doença. No início de agosto já tivemos o casos confirmados da doença em Curitiba.
Gestantes podem tomar a vacina contra o sarampo?
Não, a vacina do sarampo é contra-indicada para gestantes pois é produzida com o vírus vivo atenuado. A recomendação é que a vacinação seja feita ANTES da gestação. Portanto se você está planejando engravidar, verifique no seu cartão de vacinas se você já se vacinou.
A vacina triplice viral (sarampo, rubéola e caxumba) é disponibilizada gratuitamente no Sistema Único de Saúde (SUS) para crianças e adultos. Quem já teve a doença na infância está imune e não corre o risco de contrair novamente a doença.
Depois de receber a vacina, as mulheres devem esperar 4 semanas antes de tentar a gravidez, dado os riscos teóricos para o feto com vacinas vivas. No entanto, a vacinação com a triplice viral inadvertida no período de periconcepcional ou no início da gravidez não deve ser considerada uma indicação para o término da gravidez.
Como o sarampo é transmitido?
A transmissão ocorre diretamente, de pessoa a pessoa, geralmente por tosse, espirros, fala ou respiração, por isso a facilidade de contágio da doença. Além de secreções respiratórias ou da boca, também é possível se contaminar através da dispersão de gotículas com partículas virais no ar, que podem perdurar por tempo relativamente longo no ambiente, especialmente em locais fechados como escolas e clínicas. A doença é transmitida na fase em que a pessoa apresenta febre alta, mal-estar, coriza, irritação ocular, tosse e falta de apetite e dura até quatro dias após o aparecimento das manchas vermelhas.
Quais são os principais sintomas?
Após a infecção, os primeiros sintomas parecem em 7 a 14 dias e são febre alta, tosse, coriza e conjuntivite. Cerca de 2 a 3 dias após o início dos sintomas é possível observar as manchas de Koplik que são pontos brancos na mucosa oral, mais comumente próximo aos molares, porém podem se estender por toda a mucosa oral. Essas manchas na boca costumam preceder o aparecimento dos exantemas (lesões de pele).
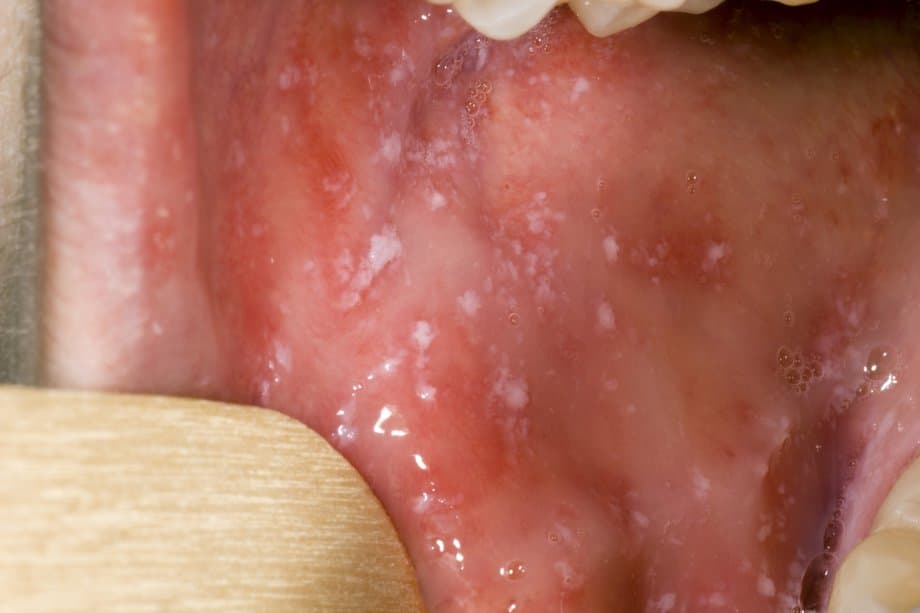
Manchas de Koplik
De 3 a 5 dias após o início dos sintomas, inicia o período exantemático da doença. Então as lesões da pele (exantemas) aparecem. São manchas avermelhadas que geralmente iniciam na cabeça (próximo ao cabelo) progredindo para face e pescoço. Em seguida descem pelo corpo em direção aos pés. Esta fase tem duração mínima de 3 dias.
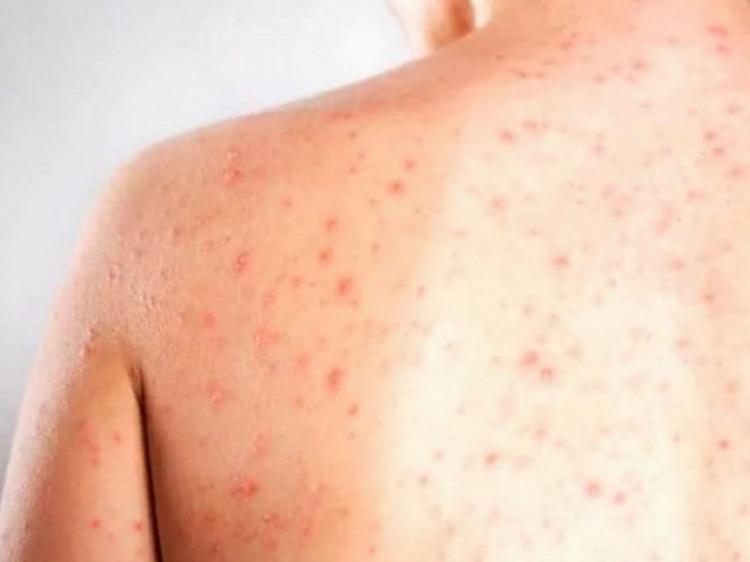
Exantema do Sarampo
Quais os riscos para a gestante?
A infecção por sarampo em mulheres grávidas está associada a vários eventos adversos. Isto inclui aumento do risco de hospitalização e pneumonia. A infecção por sarampo durante a gravidez também está associada a riscos significativos para o feto, incluindo:
- Aborto espontâneo
- Óbito fetal
- Baixo peso de nascimento
- Aumento do risco de parto prematuro
Referências
- Folha informativa – Sarampo – OPAS
- Practice Advisory: Management of Pregnant and Reproductive-Aged Women during a Measles Outbreak
- Sarampo: sintomas, transmissão, como prevenir e tratar a doença