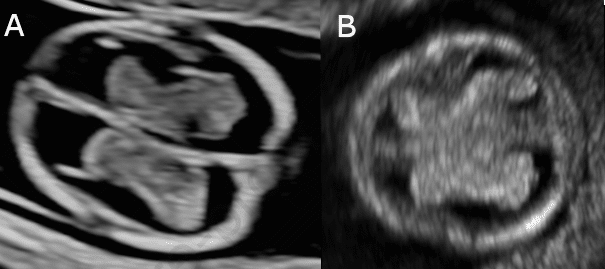
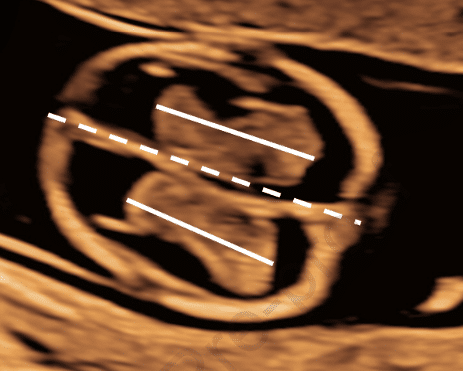
Autores: A. Khalil, A. Samara, P. O’Brien, E. Morris, T. Draycott, C. Lees, S. Ladhani
Artigo Original: Monkeypox and pregnancy: what do obstetricians need to know? Ultrasound in Obstet & Gyne, Volume: 60, Número: 1, Páginas: 22-27 (publicado em 02/07/2022)
Introdução
Um surto de varíola afetando vários países começou no início de maio de 2022 e, em 25 de maio de 2022, um total de 219 casos confirmados foram relatados em todo o mundo, com o número de casos continuando a aumentar rapidamente1. Este é o primeiro surto fora da África cuja fonte ainda não pode ser rastreada diretamente para a África Ocidental ou Central, onde esta doença é endêmica. Investigações laboratoriais confirmaram que o surto atual é devido ao clado da varíola dos macacos2-4 da África Ocidental, que tem uma taxa de mortalidade de cerca de 1%5. O clado da África Central (Bacia do Congo) tem historicamente causado doenças mais graves e também pode ser mais transmissível, com uma taxa de letalidade de até 10%.
Epidemiologia
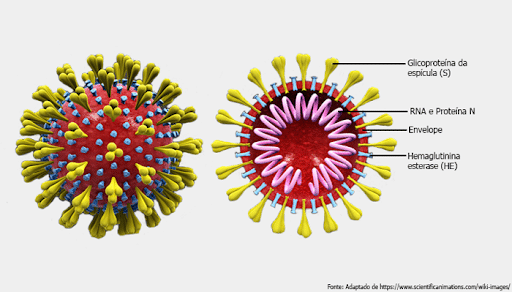
O vírus da varíola dos macacos pertence ao gênero orthopoxvirus e foi identificado pela primeira vez em macacos em 19586. O gênero orthopoxvirus inclui, entre outros, o vírus da varíola (causador da varíola), o vírus vaccinia (usado na vacina contra a varíola) e o vírus da varíola bovina. Apesar do nome, o principal hospedeiro da varíola dos macacos são os roedores e seu reservatório natural permanece desconhecido. O primeiro caso humano de varíola dos macacos foi registrado em 1970 no Congo. Desde então, a varíola dos macacos tornou-se endêmica na África Ocidental e Central; a maioria dos casos é observada na República Democrática do Congo (RDC), com milhares de casos anualmente7.
O último caso que ocorreu de forma natural de varíola foi na Somália em 1977, após o programa mundial de vacinação para erradicar a doença. Consequentemente, a vacina contra a varíola foi descontinuada no final da década de 1970. A proteção cruzada significativa que esta vacina oferecia contra a varíola dos macacos foi, portanto, perdida, e o vírus da varíola dos macacos tornou-se um patógeno mais significativo entre os seres humanos. Um grande surto de varíola que começou na Nigéria em 2017 e continua até hoje cruzou as fronteiras da Nigéria oito vezes, com pessoas infectadas transportando o vírus para vários países, incluindo o Reino Unido e os EUA8.
Incubação e Transmissão
A transmissão do vírus da varíola dos macacos para humanos pode ocorrer por mordida de animal ou contato direto com sangue, carne, fluidos corporais ou lesões cutâneas/mucosas do animal infectado. A transmissão de humano para humano por contato direto próximo e por meio de grandes gotículas exaladas é rara, mas pode ocorrer esporadicamente. A transmissão sexual também pode ser possível, embora não esteja claro se isso se deve ao contato sexual ou contato próximo durante a relação sexual5. Embora as evidências sejam limitadas e o risco de transmissão de humano para humano pareça ser baixo, bebês e crianças pequenas parecem estar em maior risco de doença grave.
Sinais, sintomas e história natural
A extensão em que a infecção assintomática por varíola dos macacos pode ocorrer é desconhecida. O período de incubação é geralmente de 6 a 13 dias, mas pode variar de 5 a 21 dias. Isto é seguido por uma fase prodrômica caracterizada por febre, suores, dores de cabeça, mialgia e fadiga. A fase de erupção cutânea geralmente começa de 1 a 3 dias após o aparecimento da febre. A erupção tende a acometer a face e extremidades, evoluindo de máculas para pápulas, vesículas, pústulas e eventualmente crostas (Figura 1). Essas lesões podem assemelhar-se às da varíola ou da varicela, mas a linfadenopatia geralmente é mais proeminente na infecção por varíola dos macacos9,10. Indivíduos imunocomprometidos são mais vulneráveis a formas mais graves da doença e têm maior taxa de letalidade.
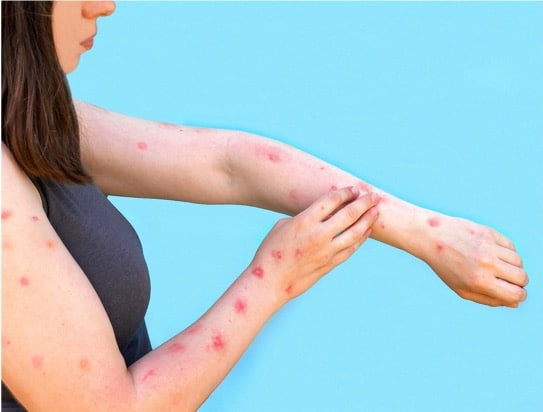
Erupção cutânea da Varíola dos Macacos
Varíola dos Macacos na Gravidez
Os dados são muito escasso sobre a infecção por varíola dos macacos na gravidez, principalmente devido aos desafios socioeconômicos e conflitos civis em muitos países em que é endêmica, o que significa que os relatos na literatura médica são raros. Não está claro se a transmissão vertical do vírus da varíola dos macacos pode ocorrer. A Organização Mundial da Saúde (OMS) relata que a transmissão da mãe para o feto pode ocorrer pela placenta (que pode levar à varíola congênita) ou por contato próximo durante e após o parto11. Um estudo observacional de uma coorte de 222 indivíduos sintomáticos internados com varíola dos macacos na República Democrática do Congo entre 2007 e 2011 incluiu quatro gestantes12. Três das quatro mulheres tiveram óbito fetal e a quarta deu à luz um bebê saudável a termo. As perdas gestacionais incluíram duas mulheres com doença moderada a grave que terminou em aborto espontâneo no primeiro trimestre; em ambos os casos, os tecidos ovulares não foram testados para a doença. A terceira mulher teve varíola dos macacos moderadamente grave com 18 semanas de gestação e teve óbito fetal. O feto apresentava características clínicas de infecção por varíola do macaco e havia evidências virológicas, histológicas e sorológicas sugerindo que o feto morreu devido à transmissão vertical desse vírus. Especificamente, o feto apresentava lesões maculopapilares cutâneas difusas na pele da cabeça, tronco e extremidades (incluindo abdome, tórax, dorso e também as palmas e plantas das mãos e pés). Havia também hidropisia fetal e hepatomegalia acentuada com ascite. Não havia malformações congênitas, deformidades ou anormalias macroscópicas na placenta, membranas ou cordão umbilical. Extensa autólise post mortem estava presente e foi consistente com óbito fetal12. Em outro relato de caso provável (não confirmado laboratorialmente), uma gestante infectada com cerca de 24 semanas de gestação deu a luz a um bebê prematuro 6 semanas depois. O bebê teve uma erupção cutânea generalizada consistente com varíola dos macacos e morreu de desnutrição 6 semanas depois10.
Os dados sobre a varíola na gravidez são claramente limitados e sujeitos a viés de notificação. Atualmente, não há evidências sobre o risco de transmissão viral para o lactente durante a amamentação, seja pelo leite materno, contato direto com lesões cutâneas maternas ou pela disseminação de grandes gotículas. É importante notar que a varíola ortopoxvírus relacionada está associada a um risco aumentado de morbidade e mortalidade materna e perinatal, incluindo óbito fetal, parto prematuro e aborto espontâneo11, 13, 14.
Diagnóstico
Se uma pessoa grávida apresentar sintomas sugestivos de varicela (como erupção cutânea ou novas lesões genitais)15, os médicos devem incluir a infecção por varíola no diagnóstico diferencial, independentemente de a pessoa ter histórico de viagem para um país da África Central ou Ocidental16. A varíola dos macacos é diagnosticada pelo teste de reação em cadeia da polimerase (PCR) de um swab viral, que pode distinguir a varíola dos macacos não apenas de outros ortopoxvírus, mas também entre os clados da África Central e da África Ocidental. Atualmente, não há teste de vírus da varíola do macaco aprovado, e a positividade na maioria dos países é confirmada por laboratórios nacionais de referência17. Em 25 de maio de 2022, a empresa farmacêutica Roche (Basileia, Suíça) anunciou que desenvolveu um kit de detecção quantitativa baseado em PCR para o vírus da varíola dos macacos18. O swab deve ser preferencialmente retirado de uma ferida aberta ou da superfície de uma vesícula, em seguida colocado em meio de cultura viral ou meio de transporte viral para ser enviado ao laboratório de virologia19. Se todas as lesões apresentarem crostas, o material da crosta deve ser raspado para um recipiente universal simples e seco. Se o paciente tiver febre, erupção cutânea disseminada, dor de garganta ou outros sintomas sistêmicos, uma amostra de sangue com EDTA e um swab da garganta também devem ser coletados (o swab da garganta deve ser enviado em meio de transporte viral). Para contatos de alto risco de um caso confirmado que apresentam sintomas sistêmicos, mas não apresentam erupção cutânea ou lesões para amostragem, deve-se coletar um swab da garganta19. Escaras, swabs e fluido aspirado da lesão são preferíveis a amostras de sangue devido à duração limitada da viremia, portanto, se houver lesões, elas devem ser priorizadas para coleta de swab.
Equipamentos de proteção individual e isolamento
Os profissionais de saúde devem usar equipamento de proteção individual (EPI) apropriado sempre que estiverem próximos de casos suspeitos ou confirmados de varíola dos macacos e seguir as práticas usadas para proteção contra vírus transmitidos pelo ar, gotículas e vírus de contato. Isso deve incluir respiradores FFP3 devidamente ajustados, luvas, bata e proteção para os olhos, como óculos de proteção ou protetor facial. Pacientes com infecção por varíola dos macacos suspeita ou confirmada por PCR devem ser isolados em uma sala de pressão negativa. Em alguns sistemas de saúde, uma vez confirmado o diagnóstico de varíola dos macacos, o paciente será transferido para um centro especializado para cuidados adicionais. Por exemplo, no Reino Unido, esta seria uma Unidade de Doenças Infecciosas de Alta Consequência.
Terapia antiviral
Atualmente, não há medicação específica para tratar a varíola, mas os antivirais cidofovir, brincidofovir e tecovirimat podem ser considerados20. O tecovirimat é aprovado pela Food and Drug Administration (FDA) dos EUA para o tratamento da varíola humana em adultos e crianças com peso mínimo de 3 kg21. Tecovirimat não foi autorizado para uso durante a gravidez, pois não há dados sobre seu uso em mulheres grávidas e os estudos em animais são insuficientes em relação à toxicidade reprodutiva22. Como o prognóstico depende de vários fatores, a orientação atual dos Centros de Controle e Prevenção de Doenças (CDC) para o tratamento da varíola dos macacos é que mulheres grávidas e lactantes podem ter alto risco de doença grave e, portanto, devem ser consideradas para tratamento após consulta ao CDC21. De acordo com o conselho do FDA, uma terapia alternativa ao brincidofovir deve ser usada para tratar a varíola durante a gravidez, se viável23; a mesma orientação provavelmente se aplica ao seu uso para a varíola dos macacos. O cidofovir é classificado como um medicamento da categoria C da FDA para gravidez porque efeitos embriotóxicos e teratogênicos foram observados em estudos com animais, incluindo restrição de crescimento e anormalidades nos tecidos moles e ósseo24. A recomendação é que o uso desse medicamento seja considerado apenas quando a mulher estiver gravemente doente.
Imunoglobulina
Durante o surto de varíola dos macacos em 2003 nos EUA, o CDC emitiu orientações para a prevenção da varíola dos macacos usando a vacina contra a varíola ou a imunoglobulina vaccinia (VIG)25. VIG é um coquetel de anticorpos purificados do sangue de indivíduos imunizados com a vacina contra a varíola. Não existem dados disponíveis sobre a eficácia do VIG no tratamento da varíola dos macacos; no entanto, o CDC aconselha que pode ser considerado para uso profilático quando indivíduos expostos à varíola dos macacos apresentam imunodeficiência grave na função das células T, nos quais a vacinação, que inclui um vírus vivo atenuado, seria contraindicada26. Embora pouco se saiba sobre a VIG na gravidez, outras imunoglobulinas têm sido extensivamente estudadas e geralmente consideradas seguras na gravidez24.
Imunização na população não grávida
Embora a imunização de rotina para a varíola tenha terminado há quase 50 anos, os idosos vacinados antes disso ainda devem ter proteção contra a varíola. Além disso, como a varíola dos macacos é em grande parte uma doença autolimitada, espera-se que adultos saudáveis se recuperem da infecção. Embora as evidências sejam limitadas, crianças e bebês parecem estar em maior risco de doença grave27.
A doença pode ser atenuada pela vacinação pós-exposição usando MVA-BN®, uma vacina de terceira geração (vivo, não replicante). No atual surto de varíola, o conselho da Agência de Segurança da Saúde do Reino Unido (UKHSA; anteriormente conhecido como Saúde Pública da Inglaterra)28 e do CDC29 é vacinar contatos de casos confirmados, incluindo profissionais de saúde, idealmente dentro de 4 dias e até 21 dias após exposição (ou seja, profilaxia pós-exposição). A administração da vacina até 14 dias pós-exposição pode não prevenir a doença, mas pode reduzir a gravidade dos sintomas29. O MVA-BN gera resposta imune protetora contra uma variedade de ortopoxvírus e é 85% eficaz na proteção contra a varíola dos macacos28.
Aprovada em 2013, a MVA-BN é comercializada na União Europeia (UE) como Imvanex30 e é a única vacina de terceira geração licenciada para imunização ativa contra varíola em adultos. O fabricante (Bavarian Nordic, Martinsried, Alemanha) ainda não solicitou uma extensão da licença da UE para incluir a imunização contra a varíola dos macacos. Nos EUA, no entanto, onde o MVA-BN é comercializado como JYNNEOS™, ele é aprovado pelo FDA para vacinação contra infecção por varíola e varíola dos macacos em adultos31.

Figura 2: Fluxograma recomendado para casos suspeitos ou confirmados de varíola dos macacos em gestantes.
Vigilância fetal
Como os dados sobre a infecção por varíola dos macacos na gravidez são limitados, o risco para o feto atualmente não é quantificável; no entanto, parece que a transmissão vertical e a morte fetal são possíveis. Portanto, até que mais dados estejam disponíveis, seria prudente adotar uma abordagem cautelosa em gestações com infecção confirmada por varíola dos macacos. Isso inclui avaliação regular (2-3 vezes ao dia) do bem-estar fetal com cardiotocografia se a idade gestacional for ≥ 26 semanas ou se a mãe não estiver bem. A avaliação ultrassonográfica do feto e da função placentária deve ser realizada regularmente durante a infecção aguda. No primeiro trimestre, isso seria para confirmar a viabilidade e oferecer triagem. No segundo trimestre, a avaliação deve incluir biometria fetal com intervalo de 10 a 14 dias, exame anatômico detalhado e medida do volume de líquido amniótico. No terceiro trimestre, a avaliação deve incluir biometria fetal com intervalo de 10 a 14 dias, exame anatômico detalhado, medida do volume de líquido amniótico e Doppler fetal (artéria umbilical e artéria cerebral média). É provável que, uma vez resolvida a infecção materna, o risco para o feto seja pequeno; no entanto, novamente, como os dados são limitados, exames fetais de 4 semanas para o resto da gravidez devem ser considerados, como precaução. Um fluxograma do manejo proposto de gestações com infecção confirmada por varíola dos macacos é mostrado na Figura 3.
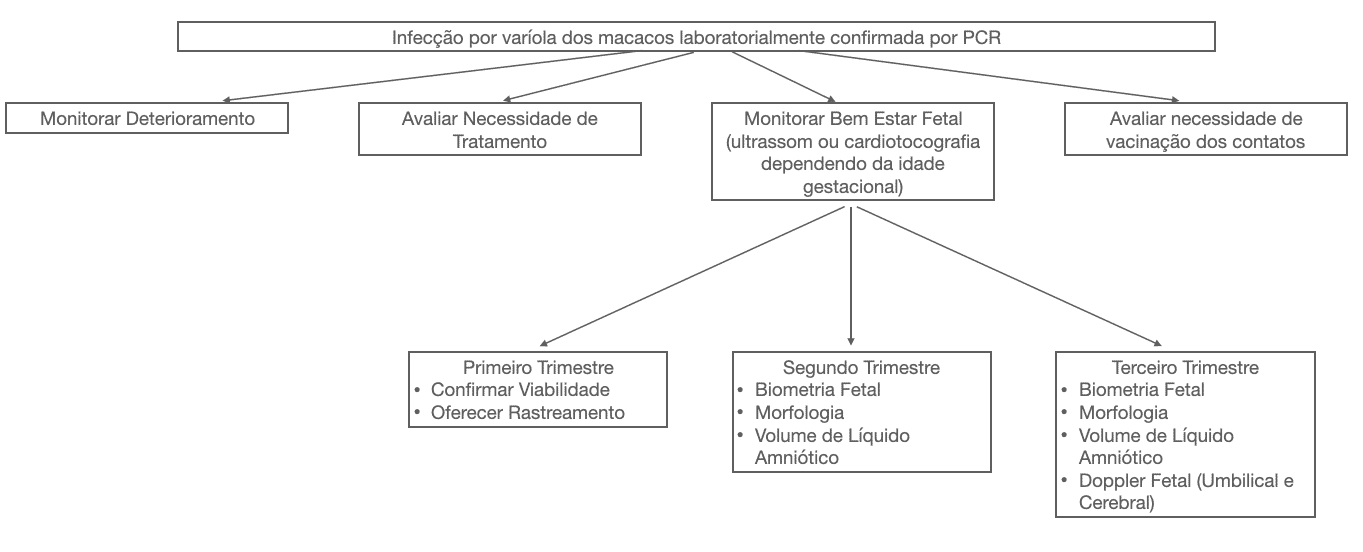
Figura 3 – Manejo proposto da infecção confirmada por varíola dos macacos na gravidez.
Momento e Via de Parto
Em geral, a infecção materna por varíola dos macacos por si só não é uma indicação para antecipar o parto, pois a maioria dos casos não é grave e é autolimitada, particularmente aqueles causados pelo clado do vírus da África Ocidental responsável pelo surto atual. Se em qualquer fase houver evidência de comprometimento fetal, ou se a vida da mãe estiver em risco, deve-se considerar o parto, levando em consideração a idade gestacional, peso fetal estimado, estado do feto e se a mãe é provável que se beneficie ou fique ainda mais comprometida com o parto (geralmente cesariana nestas circunstâncias). O sulfato de magnésio deve ser administrado para neuroproteção neonatal quando o parto prematuro for considerado, de acordo com a política da unidade. Parece improvável que um único curso de esteróides para maturação fetal antes do parto prematuro tenha um efeito adverso significativo na condição materna. No entanto, seu uso planejado deve ser discutido com o virologista e a equipe multidisciplinar mais ampla que cuida da mulher.
Não há evidências sobre o modo ideal de parto em uma mulher com infecção ativa por varíola dos macacos. É provável que a transmissão vertical seja possível, então o bebê já pode estar infectado antes do nascimento, caso em que a cesariana pode não trazer nenhum benefício. Sabe-se que o vírus pode ser transmitido pelo contato com lesões abertas da varíola dos macacos. É provável, portanto, que o trabalho de parto e/ou parto vaginal em uma mulher com lesões genitais possa levar à infecção neonatal. Dado que os bebês parecem estar em maior risco de infecção grave por varíola, se forem identificadas lesões genitais, a cesariana deve ser recomendada. Mesmo que as lesões genitais não possam ser identificadas em uma mulher com infecção confirmada ou provável por varíola, a cesariana deve ser oferecida após discussão do risco (atualmente não quantificável) de infecção neonatal, que pode ser grave. Uma proposta de tratamento de infecção suspeita ou confirmada por varíola dos macacos no trabalho de parto ou se for necessário parto urgente é mostrada no Quadro 1.

Quadro 1: Manejo proposto de infecção por varíola dos macacos suspeita ou confirmada no trabalho de parto ou se for necessário parto emergencial.
Cuidados neonatais
Há pouca evidência para orientar os cuidados neonatais após o nascimento de um bebê para uma mulher com infecção por varíola. Além do exame macroscópico, o bebê deve ser submetido ao teste de PCR viral de amostra de swab da garganta ou de quaisquer lesões que estejam presentes. O bebê deve ser isolado ao nascer de sua mãe e outros, em um único quarto, com cuidadores usando EPIs adequados. O bebê deve ser cuidadosamente monitorado quanto a sinais de comprometimento ou infecção por varíola dos macacos. Se o teste do bebê for positivo, a mãe e o bebê podem ficar juntos. Idealmente, a mãe e o bebê devem ser testados em paralelo depois disso; após o isolamento da mãe (por exemplo, dois testes de PCR negativos), a mãe e o bebê devem ficar juntos. Se uma mãe tem indicação para o teste de PCR para o vírus da varíola dos macacos, o bebê deve ser isolado até o resultado do swab.
Amamentação
A estratégia proposta para cuidados neonatais impediria que a maioria das mulheres com infecção ativa por varíola dos macacos amamentasse seus recém-nascidos. Isso parece razoável em países de alta renda, como o Reino Unido, para minimizar o risco de infecção neonatal por varíola. No entanto, em países de baixa e média renda, os benefícios da amamentação podem superar o risco potencialmente aumentado de infecção neonatal por varíola dos macacos.
Comunicação de Casos
Pouco se sabe sobre os efeitos da infecção por varíola dos macacos na gravidez, e é essencial que essa oportunidade de aprender e melhorar os cuidados não seja desperdiçada. Um registro internacional de casos em mulheres grávidas e outros indivíduos vulneráveis deve ser estabelecido sem demora. Todos os obstetras devem se esforçar para relatar casos para que, munidos de maior conhecimento, futuros surtos possam ser combatidos com mais eficácia. Isso se torna cada vez mais importante à medida que as fronteiras internacionais se confundem com o aumento do transporte de humanos e animais, de modo que a ameaça de surtos de doenças infecciosas com patógenos novos e incomuns continua a crescer.
Referências
-
- https://www.ecdc.europa.eu/en/news-events/epidemiological-update-monkeypox-multi-country-outbreak
- https://www.gov.uk/government/news/monkeypox-cases-confirmed-in-england-latest-updates
- https://virological.org/t/first-draft-genome-sequence-of-monkeypox-virus-associated-with-the-suspected-multi-country-outbreak-may-2022-confirmed-case-in-portugal/799
- https://nextstrain.org/monkeypox?c=country&p=grid
- World Health Organization. Monkeypox – United Kingdom of Great Britain and Northern Ireland. https://www.who.int/emergencies/disease-outbreak-news/item/2022-DON381
- Centers for Disease Control and Prevention. https://wwwnc.cdc.gov/travel/notices/alert/monkeypox
- Centers for Disease Control and Prevention. https://www.cdc.gov/poxvirus/monkeypox/index.html
- Beer EM, Rao VB. A systematic review of the epidemiology of human monkeypox outbreaks and implications for outbreak strategy. PLoS Negl Trop Dis 2019; 13: e0007791.
- Marennikova SS, Shelukhina EM, Matsevich GR, Ezek Z, Khodakevich LN, Zhukova OA, Yanova NN, Chekunova EV. Monkey pox in humans: current results. Acta Virol 1989; 33: 246– 253.
- Jezek Z, Gromyko AI, Szczeniowski MV. Human monkeypox. J Hyg Epidemiol Microbiol Immunol 1983; 27: 13– 28.
- World Health Organization. Monkeypox. https://www.who.int/news-room/fact-sheets/detail/monkeypox
- Mbala PK, Huggins JW, Riu-Rovira T, Ahuka SM, Mulembakani P, Rimoin AW, Martin JW, Muyembe JT. Maternal and Fetal Outcomes Among Pregnant Women With Human Monkeypox Infection in the Democratic Republic of Congo. J Infect Dis 2017; 216: 824– 828.
- Constantin CM, Martinelli AM, Foster SO, Bonney EA, Strickland OL. Smallpox: a disease of the past? Consideration for midwives. J Midwifery Womens Health 2003; 48: 258– 267.
- Waterson AP. Virus infections (other than rubella) during pregnancy. Br Med J 1979; 2: 564– 566.
- Centers for Disease Control and Prevention. https://www.cdc.gov/poxvirus/monkeypox/clinicians/clinical-recognition.html
- Centers for Disease Control and Prevention. https://www.cdc.gov/poxvirus/monkeypox/clinicians/index.html
- ECDC. Monkeypox multi-country outbreak. https://www.ecdc.europa.eu/sites/default/files/documents/Monkeypox-multi-country-outbreak.pdf
- https://www.roche.com/media/releases/med-cor-2022-05-25
- https://www.gov.uk/guidance/monkeypox-diagnostic-testing
- Centers for Disease Control and Prevention. https://www.cdc.gov/poxvirus/monkeypox/clinicians/treatment.html#Tecovirimat
- What Clinicians Need to Know About Monkeypox in the United States and Other Countries Clinician Outreach and Communication Activity (COCA) Call Thursday, May 24, 2022. https://emergency.cdc.gov/coca/ppt/2022/052422_slides.pdf
- European Medicines Agency. Assessment report. Tecovirimat SIGA. https://www.ema.europa.eu/en/documents/assessment-report/tecovirimat-siga-epar-public-assessment-report_en.pdf
- European Medicines Agency. Assessment report. Tecovirimat SIGA. https://www.ema.europa.eu/en/documents/assessment-report/tecovirimat-siga-epar-public-assessment-report_en.pdf
- Centers for Disease Control and Prevention. Interim Clinical Guidance for the Treatment of Monkeypox. https://www.cdc.gov/poxvirus/monkeypox/treatment.html
- Centers for Disease Control and Prevention. Interim guidance for use of smallpox vaccine, cidofovir, and vaccinia immune globulin (VIG) for prevention and treatment in the setting of outbreak of monkeypox infections. Atlanta, 2003. https://stacks.cdc.gov/view/cdc/25058
- https://www.cdc.gov/poxvirus/monkeypox/clinicians/treatment.html#vig
- Yinka-Ogunleye A, Aruna O, Dalhat M, Ogoina D, McCollum A, Disu Y, Mamadu I, Akinpelu A, Ahmad A, Burga J, Ndoreraho A, Nkunzimana E, Manneh L, Mohammed A, Adeoye O, Tom-Aba D, Silenou B, Ipadeola O, Saleh M, Adeyemo A, Nwadiutor I, Aworabhi N, Uke P, John D, Wakama P, Reynolds M, Mauldin MR, Doty J, Wilkins K, Musa J, Khalakdina A, Adedeji A, Mba N, Ojo O, Krause G, Ihekweazu C; CDC Monkeypox Outbreak Team. Outbreak of human monkeypox in Nigeria in 2017-18: a clinical and epidemiological report. Lancet Infect Dis 2019; 19: 872– 879.
- UK Health Security Agency. Recommendations for the use of pre and post exposure vaccination during a monkeypox incident. 2022. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/1080615/Recommendations-for-pre-and-post-exposure-vaccination-during-a-monkeypox-incident-1-june-2022.pdf
- Centers for Disease Control and Prevention. Monkeypox and Smallpox Vaccine Guidance. 2019. Monkeypox and Smallpox Vaccine Guidance | Monkeypox | Poxvirus | CDC
- https://www.ema.europa.eu/en/medicines/human/EPAR/imvanex
- https://www.fda.gov/vaccines-blood-biologics/jynneos
- European Medicines Agency. Imvanex. https://www.ema.europa.eu/en/medicines/human/EPAR/imvanex
- Ryan MA, Seward JF; Smallpox Vaccine in Pregnancy Registry Team. Pregnancy, birth, and infant health outcomes from the National Smallpox Vaccine in Pregnancy Registry, 2003-2006. Clin Infect Dis 2008; 46 (Suppl 3): S221– 226.